Sommaire de l'article
Journée de Mobilisation le 30 Mai 2024


Nous, les pharmaciens de France
Nous jouons un rôle crucial dans le système de santé. Nous sommes bien plus que des distributeurs de médicaments : nous sommes des professionnels de santé et des acteurs de proximité, surtout dans les zones rurales et fragiles. Cependant, nous faisons face à de nombreux défis qui menacent notre capacité à continuer de servir la population.
En 10 ans, la France a perdu près de 2000 pharmacies,
sur un total de 20 000 pharmacies, soit 10% des officines.
lien : https://www.mobilisationpharmaciens.fr
Nos Revendications
-
Rémunération Juste
Nous demandons une revalorisation significative de notre rémunération dès 2025. Les propositions actuelles de l'Assurance Maladie sont insuffisantes pour assurer la viabilité de nos officines.
-
Accès aux Médicaments
Les pénuries de médicaments compliquent notre tâche et affectent directement la santé de nos concitoyens. Nous devons garantir l'accès aux médicaments pour tous.
-
Maintien des Officines
Les fermetures d'officines sur les territoires fragiles mettent en péril l'accès aux soins pour de nombreuses communautés. Nous devons préserver ce service de proximité indispensable.
-
Régulation de la Vente en Ligne
La vente en ligne de médicaments sans régulation adéquate pose des risques pour la sécurité des patients et la stabilité économique de nos pharmacies. Nous demandons une régulation stricte.
-
Réforme des Études de Pharmacie
Les études doivent être adaptées aux défis contemporains. La réforme du 3ème cycle est essentielle pour préparer les futurs pharmaciens à leurs rôles complexes.
-
Reconnaissance de Nos Compétences
Nous demandons une reconnaissance officielle et une valorisation de nos compétences et de notre rôle dans la chaîne de soins, incluant des missions élargies, des responsabilités accrues et une rémunération adaptée.
Le 30 mai, les pharmacies tirent le rideau.
Grippe : pourquoi Sanofi retire du marché son vaccin surdosé Efluelda
- Le vaccin antigrippal Efluelda ne va plus être commercialisé par le géant pharmaceutique Sanofi.
- Le retrait du vaccin réservé aux plus de 65 ans est le résultat d'un désaccord entre le laboratoire et les autorités de santé sur le prix de vente.
- Cette décision n'affectera pas l'approvisionnement en vaccins antigrippaux, rassure-t-on du côté de la Direction générale de la Santé (DGS)
olémique autour d'un vaccin antigrippal. La Direction générale de la Santé (DGS) a annoncé, mardi 23 avril, l'arrêt de la commercialisation du vaccin Efluelda du laboratoire Sanofi, qui les accuse d'avoir fixé un prix trop bas. "Nous souhaitons vous informer du retrait du marché du vaccin Efluelda commercialisé par le laboratoire Sanofi dans les prochaines semaines", a annoncé l'autorité, qui dépend du ministère de la Santé, dans un message aux pharmaciens.
Ce vaccin est réservé aux plus de 65 ans, car il a été spécifiquement élaboré pour protéger les personnes les plus à risque de complications. Il est, en effet, quatre fois plus dosé que le vaccin classique contre la grippe, dit VaxigripTetra, développé par le géant pharmaceutique.
Le laboratoire pharmaceutique a justifié son choix d'arrêter la commercialisation d'Efluelda, en renvoyant la responsabilité aux autorités sanitaires qu'il accuse d'avoir fixé un prix trop bas. "Les autorités ont décidé d'établir son nouveau prix à un niveau inférieur aux coûts de production et de distribution de ce vaccin", a réagi Sanofi dans un communiqué. Le groupe, qui met aussi en avant le fait d'avoir investi 50 millions d'euros pour maintenir en France une partie de la production du vaccin, "regrette cette décision qui rend impossible la mise à disposition de ce vaccin".
Un vaccin remplacé en pharmacie
Cet affrontement s'inscrit dans un contexte de débats sur les bénéfices réels d'Efluelda par rapport aux antigrippaux classiques. Une série d'études ont établi la plus grande efficacité chez les personnes à risque, mais dans une ampleur relativement limitée. "Nous avons plus de 10 ans d'études dont de nombreuses études cliniques démontrant la supériorité d'Efluelda vs vaccins à dose standard contre la grippe, les hospitalisations attribuables à la grippe, et ses complications cardiorespiratoires", a dit Sanofi à l'AFP.
N'étant pas convaincues, les autorités sanitaires françaises refusent donc, contrairement aux États-Unis, de recommander ce vaccin plus qu'un autre pour les plus de 65 ans, ce qui justifie à leur sens de ne pas le payer plus cher.
Cette querelle a aussi lieu alors que l'industrie pharmaceutique déplore des prix trop bas fixés pour les médicaments. Sur ce plan, Sanofi a obtenu mardi l'appui d'un important syndicat de pharmaciens, la Fédération des syndicats pharmaceutiques de France (FSPF). "Face caméra, le gouvernement assure tout mettre en œuvre pour garantir l'accès aux produits de santé ; dans les faits, il s'entête dans une politique tarifaire toujours plus restrictive et dans un paradigme de santé à bas coûts", a-t-il accusé. Sollicité par l'AFP, le ministère de la Santé n'a pas réagi.
Cette décision ne devrait, en tout état de cause, pas affecter la quantité de vaccins antigrippaux disponibles puisque Sanofi promet de proposer son vaccin classique en remplacement des précommandes d'Efluelda.
coronavirus les conseils utiles

2) En complément , un article que tout le monde devrait lire: c'est très bien écrit etVirus Sars-CoV-2 : les règles à respecter au supermarché
Si vous pouvez toujours commander vos courses sur certains sites internet tel que Leclerc, Carrefour et d'autres, certains préfèrent se rendre eux-mêmes sur place. La prudence est de mise. En plus des gestes barrière comme se laver les mains très fréquemment ou tousser dans le pli de son coude, il est essentiel de prendre certaines précautions en cas de sortie au supermarché, à savoir :
- se rendre au supermarché aux heures les moins fréquentées
- amener son porte sac de course ou son propre caddie
- respecter une distance de sécurité d’au minimum 1,5 mètres avec les autres
- utiliser du gel hydro-alcoolique régulièrement
- ne pas toucher son visage avec ses mains
Quid du port des gants au supermarché ? Les experts ne recommandent pas forcément d’en porter. "Le gant fonctionne comme une deuxième peau, si j’ai un contact avec le virus, je vais garder mes gants jusqu’à ce que je les retire en arrivant chez moi… Je vais disséminer le virus de la même façon que mains nues", explique Bruno Grandbastien, président de la Société française d’hygiène hospitalière, au Monde. Il en va de même avec les masques.
Si ces accessoires vous rassurent, vous pouvez néanmoins les porter. Mais ils ne dispensent pas des gestes d'hygiène et de sécurité précédemment évoqués.
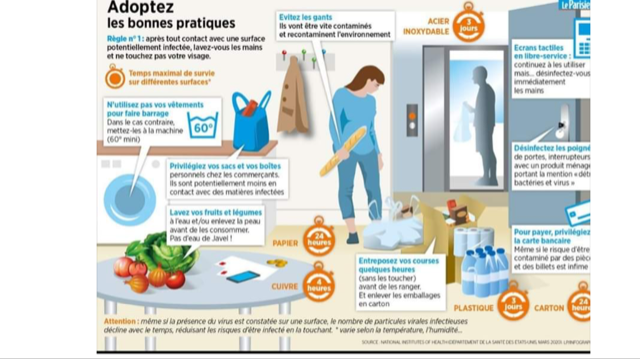
Coronavirus : les précautions à prendre en rentrant des courses
Pour éviter l’éventuelle contamination de son intérieur en rentrant chez soi avec ses sacs de courses, il est recommandé de :
- poser ses courses au sol, et non pas sur le plan de travail de la cuisine ou sur la table de la salle à manger ;
- se laver minutieusement les mains avec de l’eau et du savon dès que l’on franchi le pas de la porte ;
- retirer tous les emballages non nécessaires et les jeter immédiatement ;
- désinfecter les emballages qu’il n’est pas possible de retirer comme les pots de yaourt par exemple ;
- rincer minutieusement les aliments qui peuvent l’être, comme les fruits et les légumes, car d'autres clients ont pu les toucher ;
- passer au four les aliments qui peuvent l’être comme le pain, car un "traitement thermique à 63°C pendant 4 min permet de diviser par 10 000 la contamination d’un produit alimentaire", peut-on lire sur le site de l’Anses.
La chaleur tue le virus, l’usage d’un sèche-cheveux sur des gants en tissus ou un masque ou le repassage peut tuer les virus .Pensez dès que vous avez des symptômes rhino-pharyngés à faire une inhalation.
vraiment pertinent.
http://jdmichel.blog.tdg.ch/archive/2020/03/18/covid-19-fin-de-partie-305096.html
25 Articles (5 pages, 6 Articles par page)



